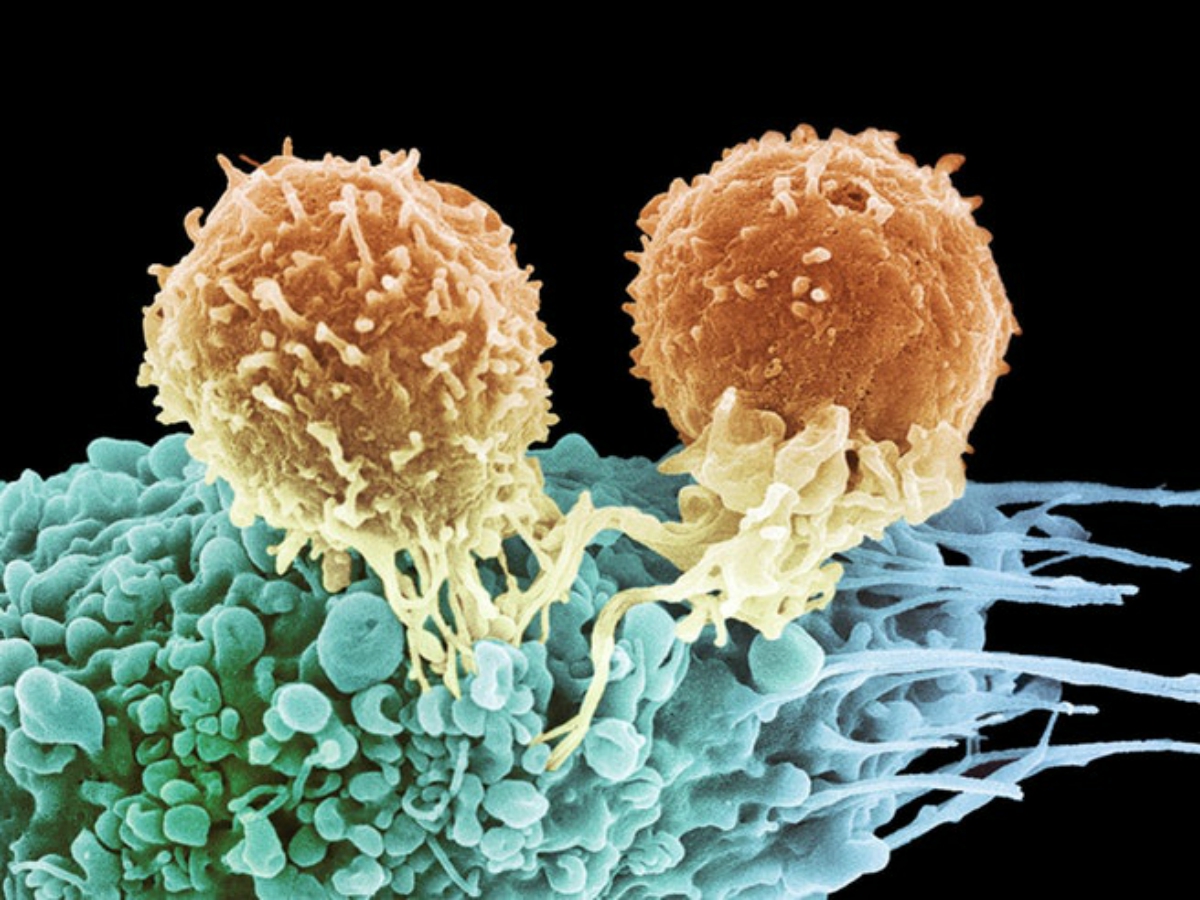
Novità in arrivo per l’immunoterapia anticancro. Da un lato Car-T a doppio bersaglio, capaci di colpire le cellule tumorali attaccandole in due punti invece che in uno. Dall’altro Car-Nk, ottenute partendo da staminali pluripotenti indotte – una riserva teoricamente infinita – che vengono ingegnerizzate e poi selezionate in modo da ricavare cellule armate contro la malattia che non sono linfociti T, bensì natural killer: la ‘fanteria’ del sistema immunitario, quella che entra in gioco per prima e che spara al nemico senza bisogno di addestramento. Un altro vantaggio non indifferente è la possibilità di pensare a un’immunoterapia cellulare ‘Car’ prodotta non di volta in volta su misura per ciascun paziente, bensì ‘prêt-à-porter’, standardizzata e pronta all’uso, riducendo tempi e costi.
 È lo scenario avveniristico tratteggiato a Orlando, in Florida, al 61° Congresso dell’American Society of Hematology (Ash). Quattro studi di fase iniziale presentati al meeting sono stati illustrati alla stampa come apripista di “un’immunoterapia cellulare di seconda generazione, che si sforza di superare i limiti dei prodotti già disponibili” contro alcune forme di leucemia e linfoma, e di ampliarne l’applicazione ad altri tumori del sangue, fra cui il mieloma multiplo. Le terapie Car-T di prima generazione, fabbricate modificando geneticamente i linfociti T del paziente in modo che esprimano il recettore Car in grado di riconoscere il cancro, “mirano principalmente alla proteina Cd19 – ricordano gli esperti – presente sulla superficie della maggior parte delle cellule B normali e maligne, nei tumori a cellule B come il linfoma. Si è dimostrato che producono remissioni a lungo termine in circa un terzo dei pazienti con linfoma a cellule B nei quali terapie precedenti hanno fallito“.
È lo scenario avveniristico tratteggiato a Orlando, in Florida, al 61° Congresso dell’American Society of Hematology (Ash). Quattro studi di fase iniziale presentati al meeting sono stati illustrati alla stampa come apripista di “un’immunoterapia cellulare di seconda generazione, che si sforza di superare i limiti dei prodotti già disponibili” contro alcune forme di leucemia e linfoma, e di ampliarne l’applicazione ad altri tumori del sangue, fra cui il mieloma multiplo. Le terapie Car-T di prima generazione, fabbricate modificando geneticamente i linfociti T del paziente in modo che esprimano il recettore Car in grado di riconoscere il cancro, “mirano principalmente alla proteina Cd19 – ricordano gli esperti – presente sulla superficie della maggior parte delle cellule B normali e maligne, nei tumori a cellule B come il linfoma. Si è dimostrato che producono remissioni a lungo termine in circa un terzo dei pazienti con linfoma a cellule B nei quali terapie precedenti hanno fallito“.
 I nuovi obiettivi ora sono tre, riassume Gary Schiller di Ucla Health: “Migliorare l’efficacia della terapia con cellule T Car, progettando prodotti capaci di attaccare obiettivi multipli; estendere l’immunoterapia cellulare ad altri tumori del sangue come il mieloma; sostituire il complesso processo necessario a ottenere le Car-T attuali con un prodotto ‘standard'”, disponibile all’uso come un normale farmaco. Una strada, quella della cosiddetta produzione ‘off-the-shelf’, percorsa dal team di Bob Valamehr della società biofarmaceutica Fate Therapeutics di San Diego, California, autore senior di un lavoro su FT596: “Una delle prime immunoterapie Car-Nk prodotte in modo standardizzato e la prima – precisa Valamehr – a contenere tre componenti anti-cancro”. Oltre al recettore Car che ‘aggancia’ Cd19, anche la proteina Cd16 che potenzia la capacità delle cellule Nk di uccidere quelle tumorali, e la proteina IL-15 che stimola FT596 a proliferare e a persistere.
I nuovi obiettivi ora sono tre, riassume Gary Schiller di Ucla Health: “Migliorare l’efficacia della terapia con cellule T Car, progettando prodotti capaci di attaccare obiettivi multipli; estendere l’immunoterapia cellulare ad altri tumori del sangue come il mieloma; sostituire il complesso processo necessario a ottenere le Car-T attuali con un prodotto ‘standard'”, disponibile all’uso come un normale farmaco. Una strada, quella della cosiddetta produzione ‘off-the-shelf’, percorsa dal team di Bob Valamehr della società biofarmaceutica Fate Therapeutics di San Diego, California, autore senior di un lavoro su FT596: “Una delle prime immunoterapie Car-Nk prodotte in modo standardizzato e la prima – precisa Valamehr – a contenere tre componenti anti-cancro”. Oltre al recettore Car che ‘aggancia’ Cd19, anche la proteina Cd16 che potenzia la capacità delle cellule Nk di uccidere quelle tumorali, e la proteina IL-15 che stimola FT596 a proliferare e a persistere.
 In fase preclinica la nuova terapia è riuscita a uccidere i globuli bianchi cancerosi in maniera paragonabile alle cellule Car-T ‘tradizionali’, e in combinazione con rituximab ha ucciso anche le cellule tumorali diventate resistenti a Car-T. FT596 ha ottenuto nel settembre scorso l’Investigational New Drug Application dalla Food and Drug Administration (Fda), e l’avvio dei test sull’uomo è previsto nel primo trimestre 2020. Sono invece già in fase clinica, i trattamenti protagonisti di altri due studi dei quattro indicati dall’Ash come esempio dei nuovi trend sull’immunoterapia cellulare. Entrambi valutano contro il mieloma multiplo nuove Car-T a doppio target: una contiene due componenti che attaccano la proteina Bcma presente quasi esclusivamente sulle plasmacellule, quelle che si ammalano nel mieloma; l’altra è progettata per colpire sia Bcma che Cd-38, un’altra proteina espressa sulla superficie delle plasmacellule.
In fase preclinica la nuova terapia è riuscita a uccidere i globuli bianchi cancerosi in maniera paragonabile alle cellule Car-T ‘tradizionali’, e in combinazione con rituximab ha ucciso anche le cellule tumorali diventate resistenti a Car-T. FT596 ha ottenuto nel settembre scorso l’Investigational New Drug Application dalla Food and Drug Administration (Fda), e l’avvio dei test sull’uomo è previsto nel primo trimestre 2020. Sono invece già in fase clinica, i trattamenti protagonisti di altri due studi dei quattro indicati dall’Ash come esempio dei nuovi trend sull’immunoterapia cellulare. Entrambi valutano contro il mieloma multiplo nuove Car-T a doppio target: una contiene due componenti che attaccano la proteina Bcma presente quasi esclusivamente sulle plasmacellule, quelle che si ammalano nel mieloma; l’altra è progettata per colpire sia Bcma che Cd-38, un’altra proteina espressa sulla superficie delle plasmacellule.
 Statunitense il primo lavoro (relatore Deepu Madduri, The Tisch Cancer Institute – Mount Sinai, New York) e cinese il secondo (Yu Hu, Union Hospital – Huazhong University of Science and Technology, Wuhan), tutti e due mostrano risultati promettenti: “Molti pazienti – riferiscono dall’Ash – hanno raggiunto la negatività di malattia minima residua”, il che significa che nel midollo osseo è rimasta meno di una cellula malata su 100 mila cellule. “Un dato che, in altre ricerche, è stato associato a un rischio inferiore di ricaduta dopo più di 3 anni“. A presentare l’ultimo trial, sempre di fase I, segnalato dall’Ash nel capitolo immunoterapia è infine Stephen J. Schuster, direttore del Programma linfomi presso l’Abramson Cancer Center dell’università della Pennsylvania, ritenuto un ‘padre’ delle Car-T. Il suo lavoro riguarda mosunetuzumab, un anticorpo bispecifico. Questa famiglia di composti sono proteine artificiali ‘bifronti’, che riconoscono la cellula tumorale da un lato e il linfocita T dall’altro.
Statunitense il primo lavoro (relatore Deepu Madduri, The Tisch Cancer Institute – Mount Sinai, New York) e cinese il secondo (Yu Hu, Union Hospital – Huazhong University of Science and Technology, Wuhan), tutti e due mostrano risultati promettenti: “Molti pazienti – riferiscono dall’Ash – hanno raggiunto la negatività di malattia minima residua”, il che significa che nel midollo osseo è rimasta meno di una cellula malata su 100 mila cellule. “Un dato che, in altre ricerche, è stato associato a un rischio inferiore di ricaduta dopo più di 3 anni“. A presentare l’ultimo trial, sempre di fase I, segnalato dall’Ash nel capitolo immunoterapia è infine Stephen J. Schuster, direttore del Programma linfomi presso l’Abramson Cancer Center dell’università della Pennsylvania, ritenuto un ‘padre’ delle Car-T. Il suo lavoro riguarda mosunetuzumab, un anticorpo bispecifico. Questa famiglia di composti sono proteine artificiali ‘bifronti’, che riconoscono la cellula tumorale da un lato e il linfocita T dall’altro.
 Il farmaco si è dimostrato efficace in pazienti con linfomi non-Hodgkin (Nhl) a cellule B resistenti o recidivanti dopo diversi trattamenti, inclusi malati precedentemente sottoposti a terapia Car- T. In questi ultimi, mosunetuzumab sembra inoltre poter ‘riattivare’ le cellule Car-T prima infuse che hanno smesso di funzionare. I tre studi di fase clinica I, evidenziano gli ematologi americani, suggeriscono anche “la possibilità che le terapie Car-T a doppio bersaglio inducano in un numero minore di pazienti una sindrome da rilascio di citochine (Crs) da moderata a grave, noto effetto avverso causato da una risposta immunitaria alle cellule T che stanno attaccando il cancro. La Crs provoca sintomi simil-influenzali come febbre, dolori muscolari e affaticamento, e nei casi più gravi può essere pericolosa per la vita“.
Il farmaco si è dimostrato efficace in pazienti con linfomi non-Hodgkin (Nhl) a cellule B resistenti o recidivanti dopo diversi trattamenti, inclusi malati precedentemente sottoposti a terapia Car- T. In questi ultimi, mosunetuzumab sembra inoltre poter ‘riattivare’ le cellule Car-T prima infuse che hanno smesso di funzionare. I tre studi di fase clinica I, evidenziano gli ematologi americani, suggeriscono anche “la possibilità che le terapie Car-T a doppio bersaglio inducano in un numero minore di pazienti una sindrome da rilascio di citochine (Crs) da moderata a grave, noto effetto avverso causato da una risposta immunitaria alle cellule T che stanno attaccando il cancro. La Crs provoca sintomi simil-influenzali come febbre, dolori muscolari e affaticamento, e nei casi più gravi può essere pericolosa per la vita“.