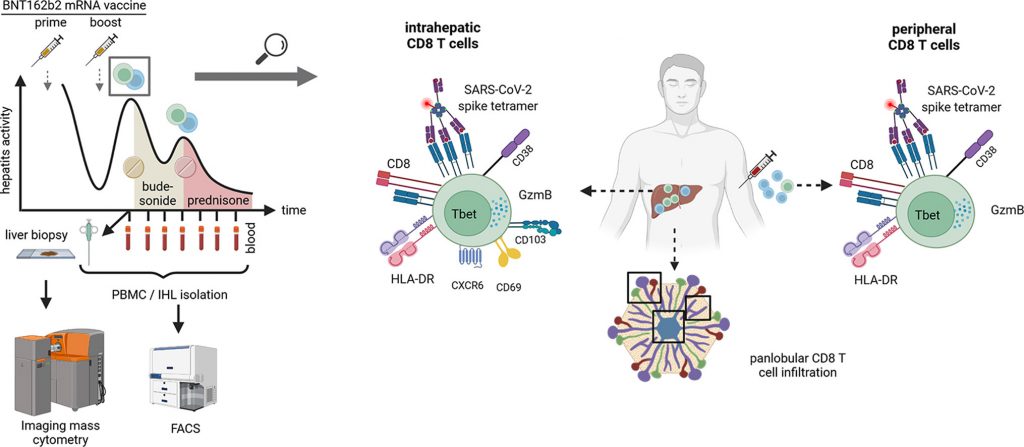
Episodi di epatite autoimmune sono stati descritti in seguito all’infezione e alla vaccinazione da SARS-CoV-2, ma la loro fisiopatologia rimane poco chiara. In uno studio pubblicato sul Journal of Hepatology, i ricercatori hanno riportato il caso di un maschio di 52 anni, che presenta epatite acuta mista epatocellularecolestatica dopo la prima dose di vaccino mRNA BNT162b2 (Pfizer) e grave epatite dopo la seconda dose. La valutazione diagnostica era compatibile con i criteri per l’epatite autoimmune (AIH). Dopo l’inizio della terapia orale con budesonide, i test di funzionalità epatica sono migliorati per un mese prima che si verificasse una ricaduta che è stata trattata con successo con prednisolone sistemico e acido ursodesossicolico. Una valutazione immunologica completa degli infiltrati infiammatori nel fegato ha rivelato la presenza di un infiltrato di cellule T CD8 citotossiche altamente attivato, inclusa una popolazione di cellule T CD8 specifiche per SARS-CoV-2 correlata con l’attivazione periferica di CD8 specifiche per SARS-CoV-2 cellule T.
Il paziente, senza una storia medica degna di nota a parte l’ipotiroidismo preesistente in terapia sostitutiva a lungo termine con levotiroxina e test di funzionalità epatica normale (LFT), ha sviluppato nausea progressiva, affaticamento, perdita di appetito e prurito con sintomi che iniziano circa 10 giorni dopo la prima dose (prime) del vaccino Pfizer. Successivamente ha sviluppato ittero e si è presentato al suo medico di base con LFT indicativo di epatite acuta mista epatocellulare/colestatica. Il paziente è stato ricoverato in un centro di cure primarie 25 giorni dopo la prima vaccinazione. L’epatite virale A, B, C ed E così come le infezioni da citomegalovirus e virus di Epstein-Barr sono state escluse dalla sierologia e/o dal test PCR. La genotipizzazione HFE non ha rivelato variazioni associate all’emocromatosi. Inoltre, non è stato riscontrato alcun consumo significativo di alcol e la sierologia autoimmune è rimasta inconcludente con la reattività borderline AMA-M2. Il paziente si è ripreso rapidamente senza una terapia specifica ed è stato dimesso con LFT in diminuzione dopo tre giorni sotto la diagnosi differenziale principale di un’epatite tossica.
Nelle due settimane successive, gli enzimi epatici sono ulteriormente diminuiti, con la normalizzazione di AST e AP e il paziente ha ricevuto la sua seconda dose (boost) del vaccino 41 giorni dopo la prima vaccinazione. Venti giorni dopo la vaccinazione boost (dpb), il paziente ha rivissuto nausea e affaticamento. I test di laboratorio hanno rivelato una ricaduta di epatite mista acuta.
“La vaccinazione COVID-19 – concludono gli autori dello studio – può suscitare una distinta epatite immuno-mediata dominante a cellule T con un patomeccanismo unico associato all’immunità residente tissutale antigene-specifica indotta dalla vaccinazione che richiede immunosoppressione sistemica”.
L’infiammazione del fegato si osserva durante l’infezione da SARS-CoV-2, ma può verificarsi anche in alcuni individui dopo la vaccinazione e condivide alcune caratteristiche tipiche della malattia epatica autoimmune. “In questo rapporto, mostriamo che le cellule T altamente attivate si accumulano e sono distribuite uniformemente nelle diverse aree del fegato in un paziente con infiammazione del fegato dopo la vaccinazione SARS-CoV-2. Inoltre, all’interno di queste cellule T che si infiltrano nel fegato, abbiamo osservato un arricchimento delle cellule T che sono reattive alla SARS-CoV-2, suggerendo che queste cellule indotte dal vaccino possono contribuire all’infiammazione del fegato in questo contesto”, concludono gli autori dello studio.