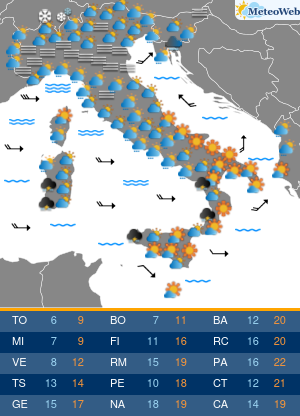
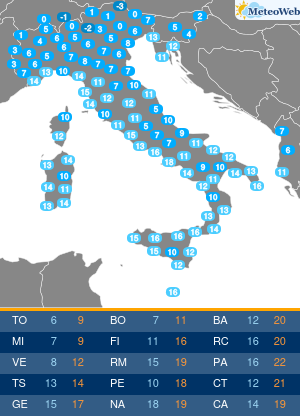
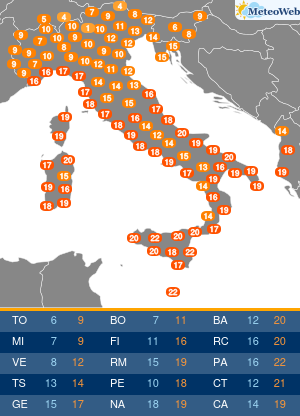
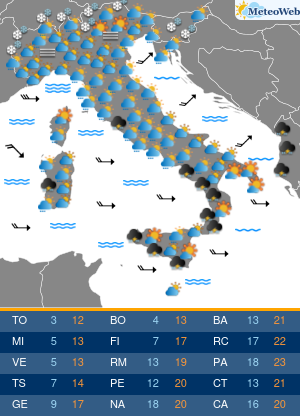
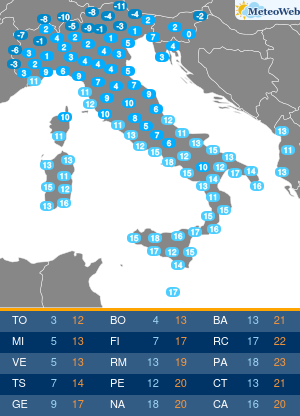
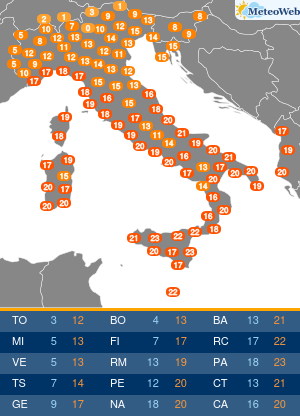
Gli USA hanno annunciato un accordo per l’acquisto di oltre 100 milioni di dosi del vaccino anti-Covid di Pfizer-BioNTech per la campagna autunnale. Il contratto da 3,2 miliardi di dollari include dosi sia per adulti che per bambini. In base a questo accordo, il governo degli Stati Uniti ha anche la possibilità di acquistare fino a 195 milioni di dosi aggiuntive, portando il numero totale di dosi potenziali a 300 milioni. Le dosi dovrebbero essere consegnate entro la fine dell’estate 2022 e continueranno nel quarto trimestre di quest’anno.
“Negli ultimi 18 mesi, abbiamo acquistato e consegnato oltre 750 milioni di dosi di vaccino contro il Covid a livello nazionale, contribuendo alla vaccinazione completa di due terzi degli adulti americani”, si legge in una nota del Dipartimento della Salute. L’annuncio, riferisce la nota, fa seguito alle raccomandazioni espresse ieri da un panel di esperti associato alla FDA, in merito alla necessità di aggiornare i vaccini attualmente a disposizione in funzione del continuo emergere di nuove varianti del coronavirus SARS-CoV-2.
“La campagna vaccinale ha rappresentato uno strumento fondamentale nel contrasto alla pandemia, e ha consentito di persone di tornare a vivere normalmente: l’amministrazione del Presidente Biden continuerà a fare tutto il necessario per garantire la disponibilità di vaccini alla popolazione“, ha commentato il Segretario alla Salute, Xavier Becerra.
“Questo accordo fornirà dosi aggiuntive per i residenti negli Stati Uniti e aiuterà a far fronte alla prossima ondata di Covid. In attesa dell’autorizzazione normativa, includerà anche un vaccino adattato per Omicron, che riteniamo importante per affrontare la variante Omicron in rapida diffusione. Apprezziamo la continua collaborazione del governo degli Stati Uniti nel nostro obiettivo condiviso di aiutare a porre fine a questa pandemia”, ha affermato Sean Marett, Chief Business e Chief Commercial Officer di BioNTech.
Il 25 giugno, Pfizer e BioNTech hanno riportato dati sulla sicurezza, la tollerabilità e l’immunogenicità di due candidati vaccini adattati a Omicron. Questi dati sono stati condivisi con le autorità di regolamentazione, inclusa la FDA, ed è prevista una richiesta di autorizzazione all’uso di emergenza negli Stati Uniti.