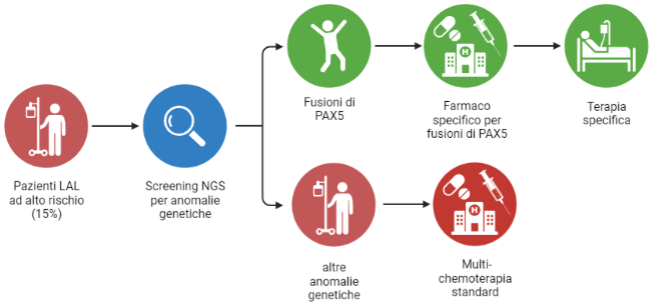
Uno studio multicentrico coordinato dalla Fondazione Tettamanti, che ha coinvolto pazienti di alcuni dei maggiori Centri clinici di Oncoematologia pediatrica italiani e l’Università di Dusseldorf (Germania), ha permesso di individuare specifiche alterazioni del gene PAX5 associate a un aumentato rischio di ricaduta e a una prognosi sfavorevole in un sottogruppo di bambini affetti da una particolare forma di leucemia linfoblastica acuta che origina da precursori delle cellule B (BCP-ALL, B Cells Precursors – Acute Lymphoblastic Leukaemia).
Questa nuova informazione permetterà di indentificare fin dal momento della diagnosi di BCP-ALL una parte di quel 15% di bambini che tendono ad andare incontro a ricadute precoci di malattia, nonostante l’impiego di protocolli di trattamento aggressivi basati sui metodi convenzionali di stima del rischio, e di offrire terapie più mirate, in funzione delle alterazioni genetiche riscontrate in PAX5 (nello specifico, il gene di fusione formato da PAX5 e diversi altri geni) che conferiscono un vantaggio di sopravvivenza alle cellule leucemiche.
Con un rilevante vantaggio aggiuntivo: nello stesso studio, i ricercatori della Fondazione Tettamanti hanno dimostrato anche che un farmaco già utilizzato in pratica clinica per la cura della fibrosi polmonare idiopatica (IPF) e in studio per l’impiego in altre malattie oncologiche è in grado di interferire con alcune delle vie molecolari che promuovono la sopravvivenza delle cellule leucemiche in cui sono coinvolti i geni di fusione di PAX5, in particolare quelle caratterizzate dall’iperattivazione della protein-chinasi LCK (Lymphocyte-specific tyrosine kinase).
Giovanni Cazzaniga, responsabile dell’unità di ricerca di ‘Genetica della leucemia’ della Fondazione Tettamanti e professore associato di Genetica medica all’Università degli Studi di Milano-Bicocca commenta: “Le alterazioni del gene PAX5 sono particolarmente frequenti in un sottogruppo di pazienti ad alto rischio, caratterizzati da un profilo di espressione genica particolare. Queste alterazioni di PAX5 hanno un significato prognostico negativo e permettono di individuare i bambini a maggior rischio di ricadute sulla base di un test genetico-molecolare”.
Nello studio, i ricercatori della Fondazione Tettamanti hanno individuato diversi geni di fusione tra PAX5 e altri geni già noti, come FBRSL1, AUTS2, DACH2, o di nuovo riscontro, come ALDH18A1, IKZF1, CDH13. Come già dimostrato in loro ricerche precedenti, alcuni di questi geni di fusione supportano la sopravvivenza delle cellule leucemiche attraverso l’over-espressione del gene della LCK.
“Ciò che più conta è che nello studio pubblicato su eBioMedicine – prosegue Giovanni Cazzaniga – abbiamo dimostrato come questa tirosinchinasi possa essere inibita da un farmaco (BIBF1120/nintedanib) autorizzato dal 2014 per il trattamento della IPF e che ha già dimostrato di possedere anche un’attività antitumorale e antiangiogenetica in trials di fase III e IV su diversi tumori solidi di difficile trattamento (carcinomi di pancreas, fegato, ovaio, polmone ecc.), nonché in studi sulla leucemia mieloide acuta (AML, Acute Myeloid Leukemia) recidivante/refrattaria dell’adulto. Il passaggio all’uso clinico non è immediato, saranno necessari ulteriori studi a supporto, ma abbiamo aperto una prospettiva”.
Inoltre, i ricercatori hanno verificato che l’inibitore della LCK agisce in modo sinergico o additivo con altri farmaci comunemente impiegati per la chemioterapia, come desametasone, vincristina e asparaginasi, indicando la possibilità di testare anche terapie di combinazione per i casi più difficili da trattare. Nel loro complesso, queste evidenze aprono la strada a una nuova opportunità terapeutica mirata per i bambini affetti da BCP-ALL con gene di fusione di PAX5, con un farmaco già disponibile sul mercato.
Lo studio è stato pubblicato sulla rivista scientifica internazionale eBioMedicine del gruppo The Lancet Discovery Science, con primo autore Grazia Fazio, ricercatrice post-doc della Fondazione Tettamanti, e coordinatore Giovanni Cazzaniga, fa parte del progetto “Passaporto genetico” finanziato principalmente dal Comitato Maria Letizia Verga ed è stato realizzato anche grazie al supporto del programma “Ricerca Finalizzata-Giovani Ricercatori” del Ministero della Salute, dell’Associazione Italiana Ricerca sul Cancro (AIRC), del progetto europeo TRANSCAN e di Fondazione Cariparo.